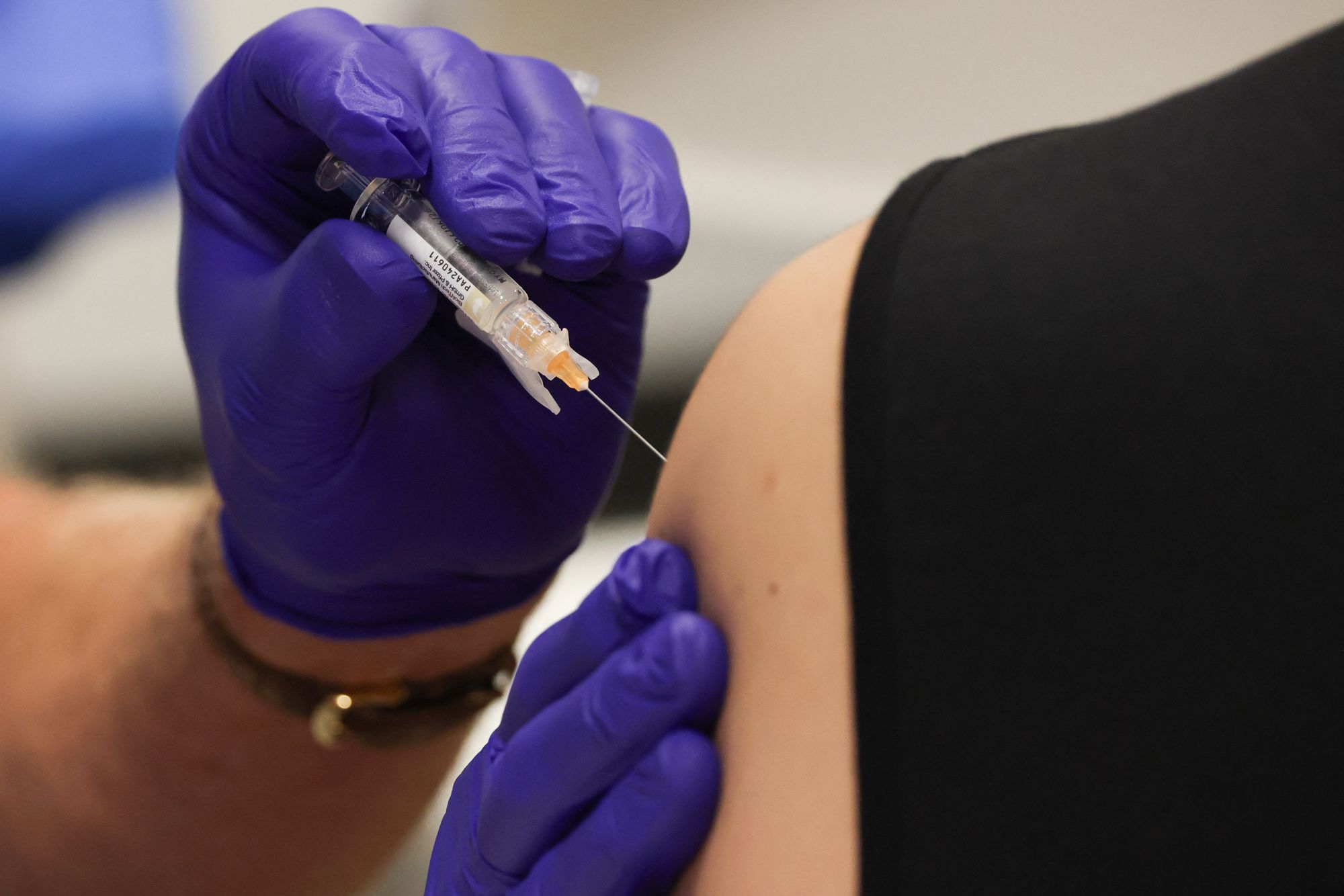
据多名了解情况的人士透露,美国食品药品监督管理局(FDA)正在考虑在新冠疫苗说明中加注“黑框警告”。该警告是 FDA 对药品和疫苗采取的最高级别安全提示,通常用于提醒可能存在的严重不良反应。这一计划尚未最终确定,但已在医学界和公共卫生领域引发广泛关注。
“黑框警告”通常置于药品处方信息的最显著位置,用于提示可能出现的死亡、危及生命或造成严重残疾的风险。历史上,此类警告曾被用于阿片类止痛药、异维A酸以及天花疫苗等产品。部分情况下,黑框警告也用于提示药品在特定人群中使用可能降低风险。
知情人士称,该计划由 FDA 首席医学与科学官、同时也是生物制品评估与研究中心(CBER)主任的维奈·普拉萨德(Vinay Prasad)推动。目前尚不清楚该警告是否仅适用于 mRNA 疫苗,或将覆盖所有新冠疫苗,也不明确是否适用于所有年龄段。FDA 目前批准了三款在美国使用的新冠疫苗,其中辉瑞和莫德纳的疫苗采用 mRNA 技术。
美国卫生与公众服务部(HHS)发言人安德鲁·尼克松表示,在 FDA 正式发布相关决定前,外界关于具体措施的说法仍属猜测。他表示,任何潜在安全问题都将通过既定的科学和监管程序进行评估。
针对相关报道,莫德纳援引其今年9月发布的声明称,其新冠疫苗的安全性持续受到公司自身、FDA 以及全球90多个国家监管机构的监测,在全球已分发超过10亿剂的情况下,未发现新的或未披露的儿童或孕妇安全问题。辉瑞也在此前声明中表示,其新冠疫苗具有良好的安全性和有效性。
多项研究显示,新冠疫苗在公共卫生层面发挥了重要作用。一项研究估计,疫苗在投入使用的第一年内在全球范围避免了近2000万例死亡。美国疾病控制与预防中心(CDC)近期发布的报告显示,在2024—2025年呼吸道病毒季节接种新冠疫苗的儿童,其因新冠病毒前往急诊或紧急护理机构的风险明显降低。
有关安全性的争议主要集中在 mRNA 疫苗可能引发的心肌炎风险。CDC 数据显示,该不良反应极为罕见,主要出现在青少年和年轻男性中,大多数患者可完全康复,且随着接种剂次间隔延长,发生率已明显下降。FDA 今年5月已要求在辉瑞和莫德纳疫苗的说明中扩大关于心肌炎和心包炎风险的提示范围。
此次计划引发部分公共卫生专家的担忧,主要集中在决策透明度和科学评估流程上。多名专家指出,目前尚未看到支持设立黑框警告的公开数据,也未召开独立专家委员会进行评估。十余名前 FDA 局长此前在《新英格兰医学杂志》发表联名公开信,对 FDA 在疫苗安全问题上的最新表述表示关切。
此外,围绕新冠疫苗的讨论也与当前美国政府内部的政策分歧有关。现任卫生与公众服务部部长罗伯特·F·肯尼迪二世长期对疫苗持批评态度,其相关立场受到部分公共卫生专家质疑。截至目前,FDA 尚未就新冠疫苗是否加注“黑框警告”作出正式宣布,相关讨论仍在持续。
未经允许不得转载:城市新闻网icitynews » FDA拟对新冠疫苗加注“黑框警告” 引发公共卫生专家关注








































