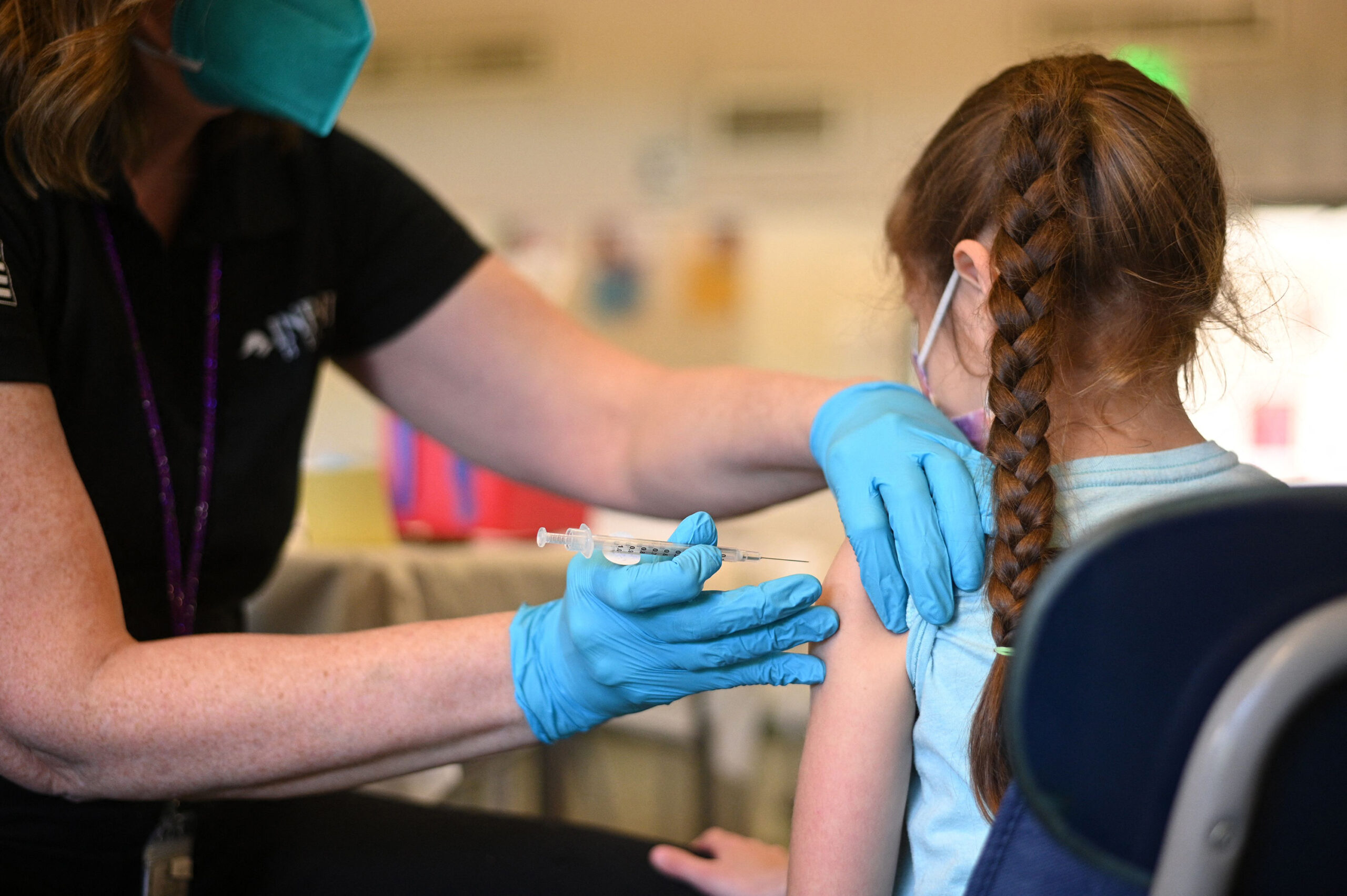
Moderna公司上周表示,该公司正在为其用于6个月至5岁儿童的Covid-19疫苗向美国食品和药物管理局寻求紧急使用授权。Moderna公司首席执行官斯蒂芬-班塞尔(Stéphane Bancel)表示:“我们相信mRNA-1273将能够安全地保护这些儿童免受新冠病毒的影响,这对我们继续对抗COVID-19非常重要。”在美国,目前没有任何Covid-19疫苗被授权用于5岁以下的儿童——大约有1800万名儿童——而且潜在授权的时间表还不清楚。Moderna公司的官员表示,预计美国食品和药物管理局会迅速采取行动,而辉瑞公司的一位官员表示,如果该疫苗获得授权,它们的低龄儿童疫苗也可能会在6月上市。
美国食品和药物管理局生物制品评估和研究中心主任彼得-马克斯博士(Dr. Peter Marks)本周称低龄儿童疫苗是 “我们最优先考虑的事项之一”,但他承认FDA仍需要疫苗制造商提供完整的申请数据以完成更仔细更认真的审查。美国食品和药物管理局将要求其独立的疫苗顾问也对低龄儿童的疫苗进行评估,马克斯博士说FDA将在下周公布咨询委员会会议的时间表。
Moderna的疫苗结果
3月下旬,Moderna宣布了一项临床试验的结果,该试验包括2500名6个月至24个月的儿童和4200名2至5岁的儿童。该公司表示,两剂25微克的疫苗在幼儿中产生的免疫反应与两剂100微克的18至25岁的成年人相似。Moderna公司首席医疗官保罗-伯顿(Paul Burton)博士说到:“我们的数据展现出了非常良好的结果,这是非常令人放心的。这些疫苗对这个年龄段的人来说是非常安全的。” 最常见的疫苗反应是注射部位的疼痛和发烧。但在研究中并没有出现心脏炎症或心肌炎的病例。心脏炎症一直是mRNA疫苗极为罕见的副作用。心肌炎在Covid-19感染后比接种疫苗后更常见。
3月份宣布的结果大多是在Omicron变种波段收集的,包括Covid-19的家庭测试。因此,该公司表示,这些疫苗对儿童的效果看起来不如对较大年龄组的效果明显。Moderna公司上周四提交的数据将分析仅限于通过PCR测试确认的阳性病例。在修订后的分析中,疫苗对预防6个月至2岁以下儿童的症状有51%的效果;对预防2至5岁儿童的症状有37%的效果。该公司表示,这些疗效估计与成人在两剂Moderna疫苗后的疗效相似。
辉瑞/BioNTech公司为幼儿研制的Covid-19疫苗也不尽如人意。在临床试验中,两个3微克的剂量似乎没有为2至4岁的儿童产生与年轻成人相同程度的免疫力,这促使该公司考虑为6个月至4岁的儿童提供第三剂量。美国食品和药物管理局也推迟了对这些疫苗的审查,直到该公司提交关于第三剂量的数据。
低龄儿童疫苗的下一步是什么?
美国食品和药物管理局将评估Moderna公司提交的材料,并表示将召集其疫苗和相关生物制品咨询委员会,对低龄儿童的疫苗授权进行权衡。如果FDA授权注射,美国疾病控制和预防中心的疫苗顾问将投票决定是否应该授权。然后,CDC主任将需要在注射疫苗前签署疫苗建议。美国国家过敏和传染病研究所所长福奇博士说,FDA正在权衡是否同时考虑对Moderna和辉瑞/BioNTech Covid-19疫苗进行紧急使用授权,而不是分别考虑。辉瑞公司表示,第三个剂量的疫苗的数据将在本月公布。辉瑞公司首席执行官补充道,如果美国食品和药物管理局授权,低龄儿童的疫苗可能在6月上市。
未经允许不得转载:城市新闻网icitynews » Moderna为5岁以下儿童寻求新冠疫苗紧急授权,FDA正在审查数据!