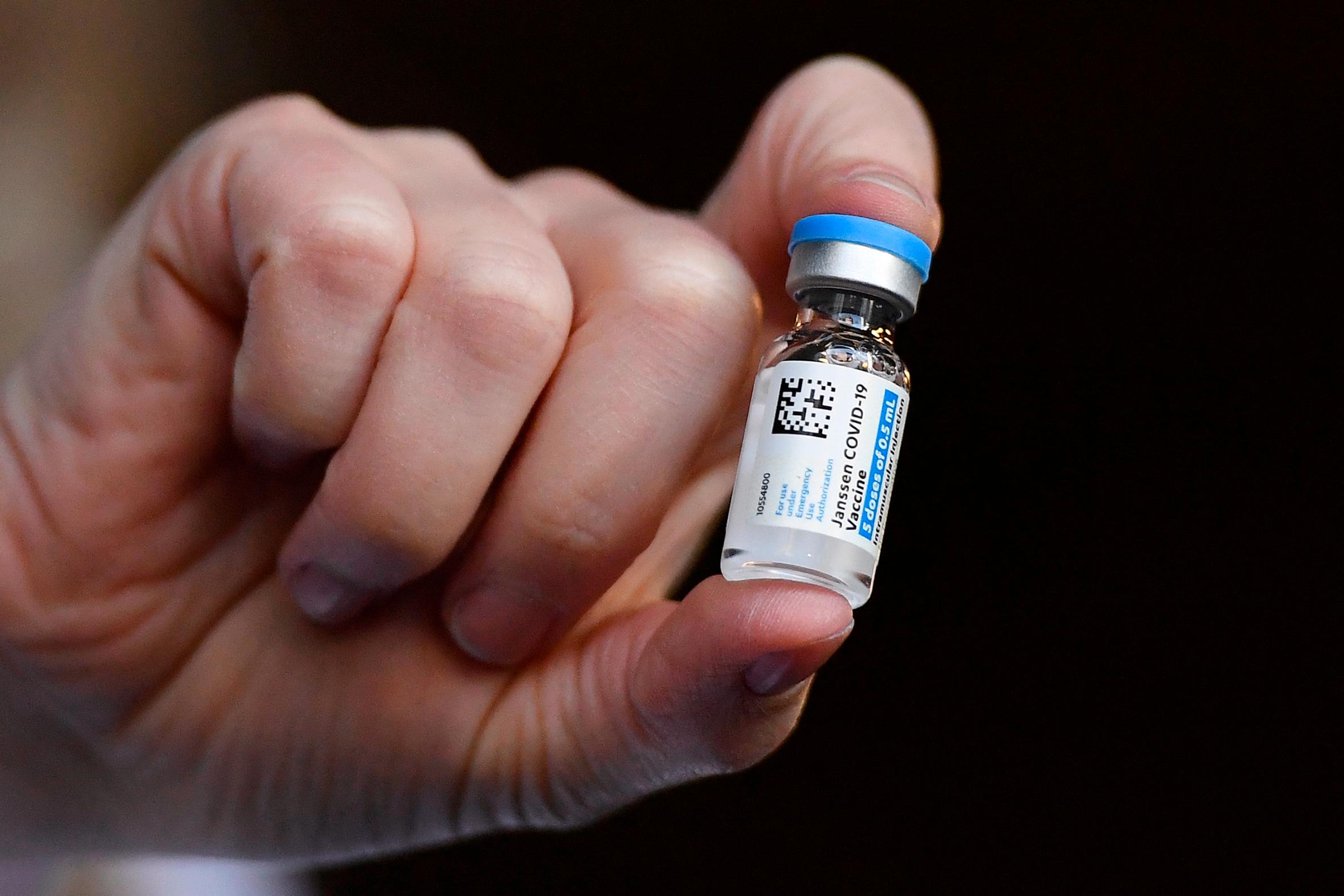
美国监管机构周三表示,巴尔的摩工厂签约制造的强生COVID-19疫苗没有遵循正确的制造程序,且由于其员工培训不足,导致材料污染。
美国食品药品监督管理局(FDA)发布了一份声明和一份长达13页的报告,详细介绍了对这家闲置的Emergent Biosciences工厂的检查结果。
机构检查人员表示,强生单次疫苗的原料药材被污染,这一批原料足以生产约1500万剂强生疫苗。
检验报告中指出的其他问题还包括:油漆剥落、工厂地板和墙壁上有黑色和棕色残留物、清洁不足以及员工未遵循防止污染的程序等。
Emergent和强生公司均在周三表示,他们正在努力尽快解决问题。目前,此批工厂生产的疫苗尚未被分发。
目前,由于政府卫生官员正在着手调查强生疫苗是否与罕见的血凝块有关,强生疫苗在美国被停止使用。在美国使用的近800万剂强生疫苗均来自欧洲。
根据FDA的要求,巴尔的摩工厂于上周停止生产。该机构尚未获得紧急批准,这是分发工厂生产的任何疫苗材料之前所必须达到的标准。
该机构说,紧急情况下生产的所有疫苗都将被存储,并将接受FDA的进一步测试。
未经允许不得转载:城市新闻网icitynews » FDA检查发现:巴尔的摩工厂生产的强生疫苗存在问题

































